Skandium, med elementsymbolet Sc og atomnummer 21, er lettløselig i vann, kan samhandle med varmt vann og mørkner lett i luften. Hovedvalensen er +3. Den blandes ofte med gadolinium, erbium og andre elementer, med lavt utbytte og et innhold på omtrent 0,0005 % i jordskorpen. Scandium brukes ofte til å lage spesialglass og lette høytemperaturlegeringer.
For tiden er de påviste scandiumreservene i verden bare 2 millioner tonn, hvorav 90–95 % finnes i bauxitt-, fosforitt- og jern-titanmalm, og en liten del i uran-, thorium-, wolfram- og sjeldne jordartsmalmer, hovedsakelig distribuert i Russland, Kina, Tadsjikistan, Madagaskar, Norge og andre land. Kina er svært rikt på scandiumressurser, med enorme mineralreserver knyttet til scandium. I følge ufullstendig statistikk er scandiumreservene i Kina omtrent 600 000 tonn, som finnes i bauxitt- og fosforittforekomster, porfyr- og kvartsårewolframforekomster i Sør-Kina, sjeldne jordartsmalmforekomster i Bayan Obo i Indre Mongolia og Panzhihua vanadium-titanmagnetittforekomster i Sichuan.
På grunn av knappheten på scandium er også prisen på scandium svært høy, og på det meste var scandiumprisen oppblåst til 10 ganger gullprisen. Selv om scandiumprisen har falt, er den fortsatt fire ganger gullprisen!
Oppdage historie
I 1869 la Mendeleev merke til et gap i atommasse mellom kalsium (40) og titan (48), og forutså at det også fantes et uoppdaget mellomliggende atommasseelement her. Han forutså at oksidet er X₂OÅ. Scandium ble oppdaget i 1879 av Lars Frederik Nilson ved Uppsala universitet i Sverige. Han utvant det fra den svarte sjeldne gullgruven, en kompleks malm som inneholder 8 typer metalloksider. Han har utvunnetErbium(III)oksidfra svart sjelden gullmalm, og utvunnetYtterbium(III)oksidfra dette oksidet, og det finnes et annet oksid av et lettere grunnstoff, hvis spekter viser at det er et ukjent metall. Dette er metallet forutsagt av Mendeleev, hvis oksid erSc₂O₃Selve scandiummetallet ble produsert fraSkandiumkloridved elektrolytisk smelting i 1937.
Mendeleev
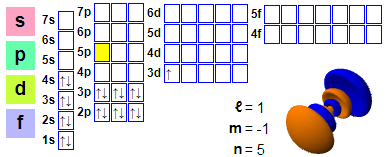
Elektronkonfigurasjon
Elektronkonfigurasjon: 1s² 2s² 2p6 3s² 3p6 4s² 3d1
Scandium er et mykt, sølvhvitt overgangsmetall med et smeltepunkt på 1541 ℃ og et kokepunkt på 2831 ℃.
I en betydelig periode etter oppdagelsen ble bruken av scandium ikke demonstrert på grunn av vanskelighetene med produksjon. Med den økende forbedringen av separasjonsmetoder for sjeldne jordartsmetaller, finnes det nå en moden prosessflyt for rensing av scandiumforbindelser. Fordi scandium er mindre alkalisk enn yttrium og lantanid, er hydroksidet det svakeste, så det blandede mineralet som inneholder scandium, som inneholder sjeldne jordartsmetaller, vil bli separert fra det sjeldne jordartsmetallet ved hjelp av "trinnvis utfelling"-metoden når scandium(III)-hydroksid behandles med ammoniakk etter å ha blitt overført til løsning. Den andre metoden er å separere scandiumnitrat ved polar dekomponering av nitrat. Fordi scandiumnitrat er det enkleste å dekomponere, kan scandium separeres. I tillegg er omfattende utvinning av medfølgende scandium fra uran, thorium, wolfram, tinn og andre mineralforekomster også en viktig kilde til scandium.
Etter å ha oppnådd en ren scandiumforbindelse, omdannes den til ScCl₃Å og smeltes sammen med KCl og LiCl. Den smeltede sinken brukes som katode for elektrolyse, noe som får scandium til å utfelles på sinkelektroden. Deretter fordampes sinken for å få metallisk scandium. Dette er et lett sølvhvitt metall med svært aktive kjemiske egenskaper, som kan reagere med varmt vann for å generere hydrogengass. Så metallet scandium du ser på bildet er forseglet i en flaske og beskyttet med argongass, ellers vil scandium raskt danne et mørkegult eller grått oksidlag, og miste sin skinnende metalliske glans.
Bruksområder
Belysningsbransjen
Bruksområdet for scandium er konsentrert i svært lyse retninger, og det er ingen overdrivelse å kalle det Lysets sønn. Scandiums første magiske våpen kalles scandiumnatriumlampe, som kan brukes til å bringe lys til tusenvis av husholdninger. Dette er et elektrisk metallhalogenidlys: pæren er fylt med natriumjodid og scandiumtrijodid, og scandium- og natriumfolie tilsettes samtidig. Under høyspenningsutladning sender scandiumioner og natriumioner henholdsvis ut lys med sine karakteristiske emisjonsbølgelengder. Spektrallinjene for natrium er 589,0 og 589,6 nm, to berømte gule lys, mens spektrallinjene for scandium er 361,3~424,7 nm, en serie med nær ultrafiolett og blått lys. Fordi de komplementerer hverandre, er den generelle lysfargen som produseres hvitt lys. Det er nettopp fordi scandiumnatriumlamper har egenskapene høy lyseffektivitet, god lysfarge, strømsparing, lang levetid og sterk duggbrytende evne at de kan brukes mye til TV-kameraer, torg, idrettsanlegg og veibelysning, og er kjent som tredje generasjons lyskilder. I Kina blir denne typen lampe gradvis promotert som en ny teknologi, mens i noen utviklede land ble denne typen lampe mye brukt så tidlig som på 1980-tallet.
Scandiums andre magiske våpen er solcelleceller, som kan samle lys spredt på bakken og omdanne det til elektrisitet for å drive det menneskelige samfunnet. Scandium er det beste barrieremetallet i metallisolatorer, halvledersilisiumsolceller og solceller.
Det tredje magiske våpenet kalles γA-strålekilde. Dette magiske våpenet kan skinne sterkt på egenhånd, men denne typen lys kan ikke mottas av det blotte øye. Det er en høyenergisk fotonstrøm. Vi utvinner vanligvis 45Sc fra mineraler, som er den eneste naturlige isotopen av scandium. Hver 45Sc-kjerne inneholder 21 protoner og 24 nøytroner. 46Sc, en kunstig radioaktiv isotop, kan brukes som γ-strålingskilde, eller sporstoffatomer kan også brukes til strålebehandling av ondartede svulster. Det finnes også bruksområder som yttrium, gallium og scandium, granatlaser.Skandiumfluoridglass infrarød optisk fiber og scandiumbelagt katodestrålerør på TV. Det ser ut til at scandium er født med lysstyrke.
Legeringsindustrien
Scandium i sin elementære form har blitt mye brukt til doping av aluminiumslegeringer. Så lenge noen få tusendeler av scandium tilsettes aluminium, vil en ny Al3Sc-fase dannes, som vil spille en metamorfoserolle i aluminiumslegering og føre til at legeringens struktur og egenskaper endres betydelig. Tilsetning av 0,2 % ~ 0,4 % Sc (som egentlig er lik andelen salt som tilsettes i stekte grønnsaker hjemme, bare litt er nødvendig) kan øke legeringens omkrystalliseringstemperatur med 150-200 ℃, og forbedre høytemperaturstyrken, strukturell stabilitet, sveiseytelse og korrosjonsmotstand betydelig. Det kan også unngå sprøhetsfenomenet som lett kan oppstå under langvarig arbeid ved høye temperaturer. Aluminiumslegering med høy styrke og høy seighet, ny høyfast korrosjonsbestandig sveisbar aluminiumslegering, ny høytemperatur aluminiumslegering, høyfast nøytronbestrålingsbestandig aluminiumslegering, etc., har svært attraktive utviklingsmuligheter innen luftfart, luftfart, skip, kjernereaktorer, lette kjøretøy og høyhastighetstog.
Scandium er også en utmerket modifikator for jern, og en liten mengde scandium kan forbedre styrken og hardheten til støpejern betydelig. I tillegg kan scandium også brukes som tilsetningsstoff i høytemperatur wolfram- og kromlegeringer. I tillegg til å lage bryllupsklær for andre, har scandium selvfølgelig et høyt smeltepunkt og tettheten er lik aluminium, og brukes også i lettvektslegeringer med høyt smeltepunkt som scandium-tianlegering og scandium-magnesiumlegering. På grunn av den høye prisen brukes det imidlertid vanligvis bare i avanserte produksjonsindustrier som romferger og raketter.
Keramisk materiale
Scandium, et enkeltstående stoff, brukes vanligvis i legeringer, og oksidene spiller en viktig rolle i keramiske materialer på lignende måte. Det tetragonale zirkoniumoksid-keramiske materialet, som kan brukes som elektrodemateriale for fastoksidbrenselceller, har en unik egenskap der konduktiviteten til denne elektrolytten øker med økende temperatur og oksygenkonsentrasjon i miljøet. Krystallstrukturen til dette keramiske materialet i seg selv kan imidlertid ikke eksistere stabilt og har ingen industriell verdi. Det er nødvendig å dope noen stoffer som kan fikse denne strukturen for å opprettholde dens opprinnelige egenskaper. Å tilsette 6~10 % scandiumoksid er som en betongstruktur, slik at zirkoniumoksid kan stabiliseres på et firkantet gitter.
Det finnes også tekniske keramiske materialer som høyfast og høytemperaturbestandig silisiumnitrid som fortettingsmidler og stabilisatorer.
Som en fortettingsmiddel,Skandiumoksidkan danne en ildfast fase Sc2Si2O7 ved kanten av fine partikler, og dermed redusere høytemperaturdeformasjonen av ingeniørkeramikk. Sammenlignet med andre oksider kan det bedre forbedre de mekaniske høytemperaturegenskapene til silisiumnitrid.
Katalytisk kjemi
Innen kjemiteknikk brukes scandium ofte som katalysator, mens Sc₂O₃ kan brukes til dehydrering og deoksidering av etanol eller isopropanol, dekomponering av eddiksyre og produksjon av etylen fra CO og H₂. Pt₃Al-katalysatoren som inneholder Sc₂O₃ er også en viktig katalysator for rensing og raffinering av tungoljehydrogenering i petrokjemisk industri. I katalytiske krakkingsreaksjoner som kumen, er aktiviteten til Sc-Y-zeolittkatalysatoren 1000 ganger høyere enn for aluminiumsilikatkatalysatoren. Sammenlignet med noen tradisjonelle katalysatorer vil utviklingsutsiktene for scandiumkatalysatorer være svært lyse.
Atomkraftindustrien
Å tilsette en liten mengde Sc2O3 til UO2 i kjernebrensel i høytemperaturreaktorer kan unngå gittertransformasjon, volumøkning og sprekkdannelser forårsaket av omdanning av UO2 til U3O8.
Brenselcelle
På samme måte vil tilsetning av 2,5 % til 25 % scandium til nikkel-alkalibatterier øke levetiden deres.
Landbruksavl
I landbruket kan frø som mais, rødbeter, erter, hvete og solsikke behandles med scandiumsulfat (konsentrasjonen er vanligvis 10⁻³ ~ 10⁻³ mol/L, forskjellige planter vil ha forskjellig), og den faktiske effekten av å fremme spiring er oppnådd. Etter 8 timer økte tørrvekten til røtter og knopper med henholdsvis 37 % og 78 % sammenlignet med frøplanter, men mekanismen er fortsatt under studier.
Fra Nielsens oppmerksomhet på gjelden av atommassedata til i dag, har scandium bare vært en del av folks synsfelt i hundre eller tjue år, men det har nesten ligget på benken i hundre år. Det var ikke før den kraftige utviklingen av materialvitenskap på slutten av forrige århundre at det ga ham vitalitet. I dag har sjeldne jordartsmetaller, inkludert scandium, blitt hete stjerner innen materialvitenskap, og spiller stadig skiftende roller i tusenvis av systemer, gir mer bekvemmelighet til livene våre hver dag og skaper økonomisk verdi som er enda vanskeligere å måle.
Publisert: 29. juni 2023